원자는 끊임없이 움직이고 있지만, DFT는 모든 것을 0 K에서 정지시킨다. "자발적인" 반응, 생성, 또는 합성을 정확하게 기술하려면 내부 에너지가 아닌 자유 에너지가 필요하다.
불균일 촉매에서의 자유 에너지
EDFT에서 G(T, P, U)까지
목차
왜 자유 에너지가 중요한가
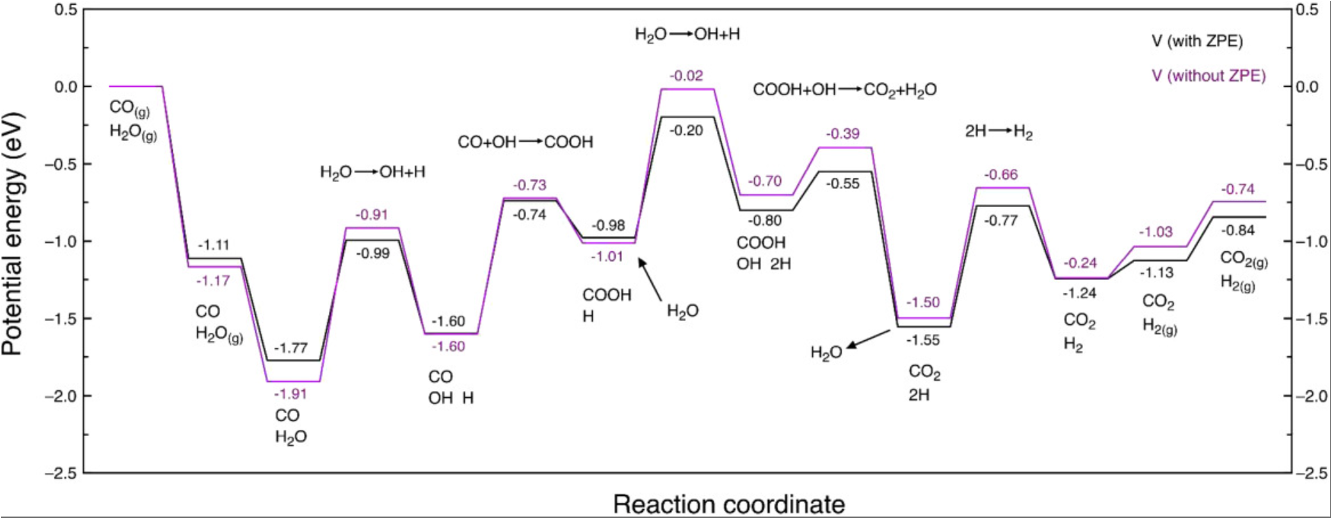
퍼텐셜 에너지 다이어그램의 문제점
현실적인 모델링을 위해

퍼텐셜 에너지 다이어그램이 틀릴 때
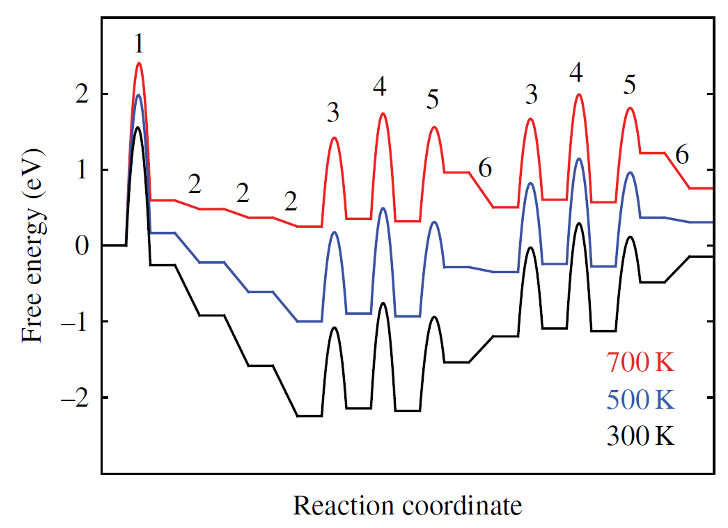
NH3 합성 — 부호 반전 (700 K)
Pt 위의 CO — 엔트로피가 지배
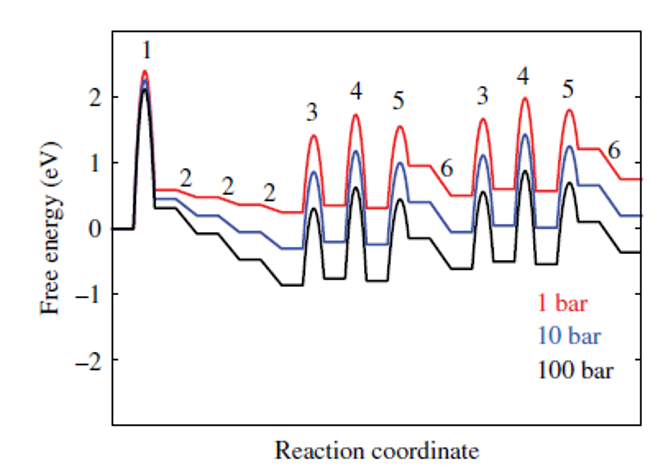
- 평형 피복률 θi(T, P)
- 에너지 스팬 모델을 통한 TOF
- 선택성: 생성물은 ΔE가 아닌 ΔG에 의해 결정됨
- TST: $k = \frac{k_B T}{h} e^{-\Delta G_{\text{TS}}/k_B T}$
활성과 선택성은 자유 에너지에 민감하다
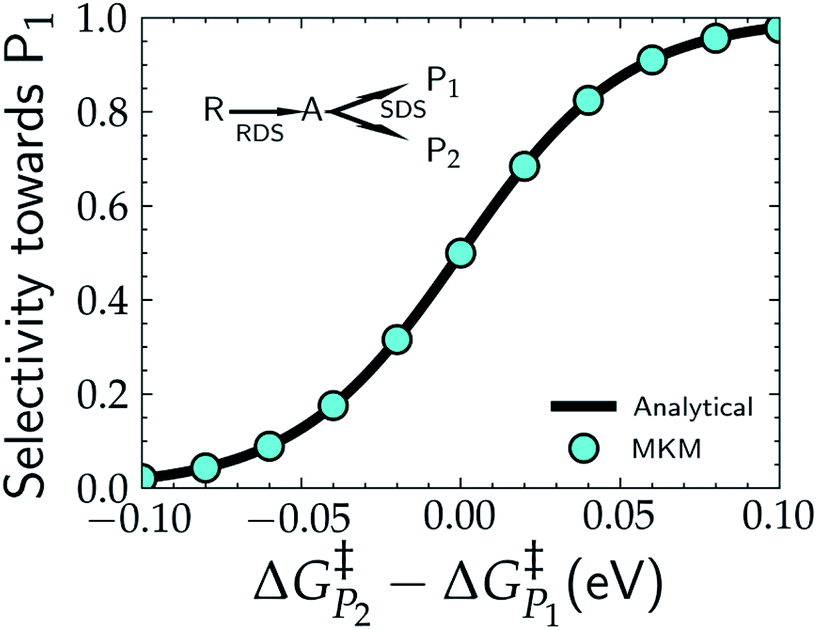
선택성은 $\Delta G_{P_2}^{\ddagger} - \Delta G_{P_1}^{\ddagger}$의 $\pm 0.05$ eV 범위 내에서 급격하게 전환된다
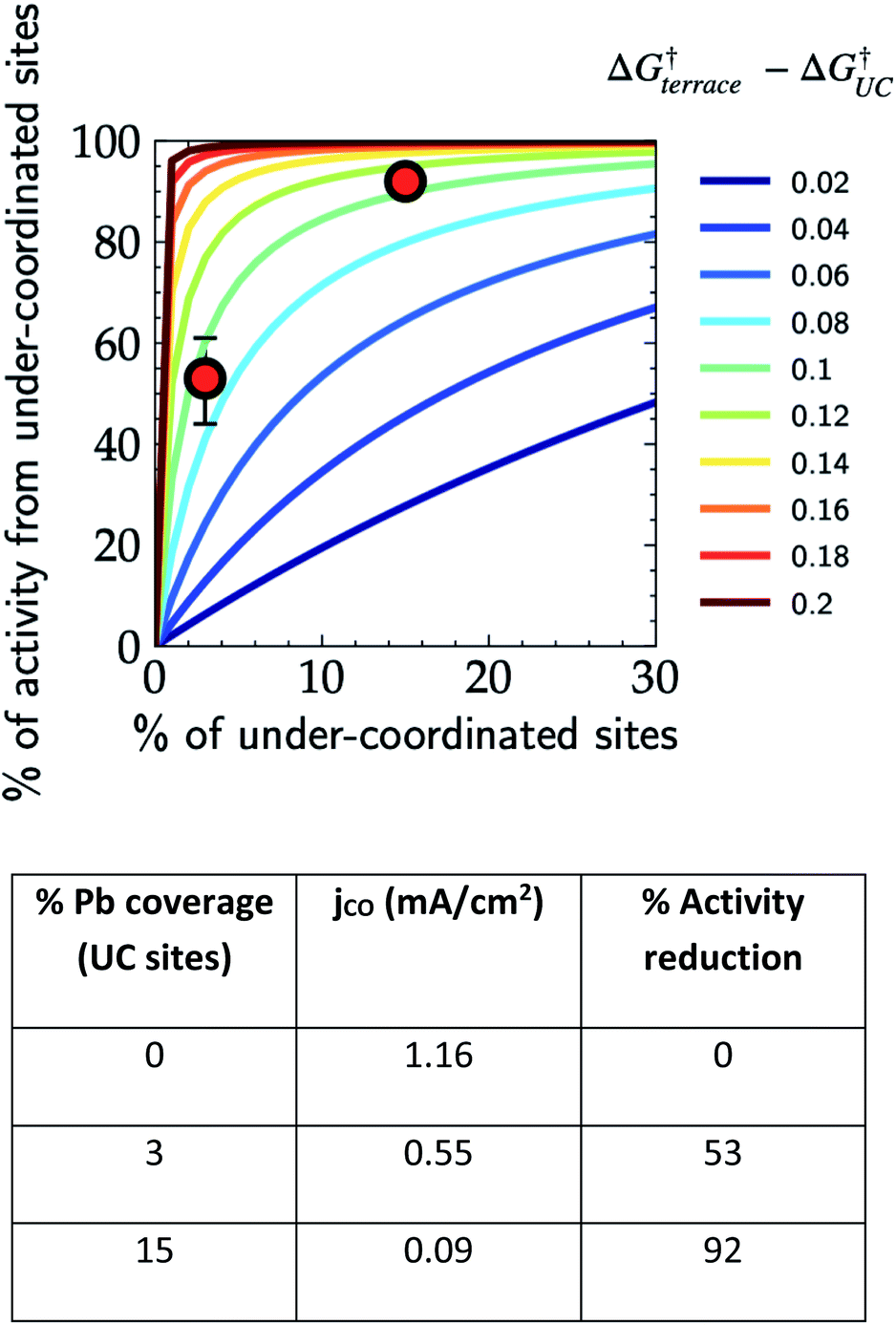
저배위 사이트의 전체 활성에 대한 기여도 대 풍부도 및 $\Delta G_{\text{terrace}}^{\dagger} - \Delta G_{\text{UC}}^{\dagger}$. 빨간 마커: Au(111)에서 Pb-UPD를 이용한 CO2RR, −0.6 V vs. RHE.
그림 출처: Govindarajan, Kastlunger, Heenen & Chan, Chem. Sci. 2022, 13, 14–26. DOI: 10.1039/D1SC04775B
ZPE와 엔트로피
양자 바닥 상태와 열적 앙상블
영점 에너지 (ZPE): 물리학부터
$E_{\min} = \tfrac{1}{2}h\nu$는 퍼텐셜 우물 바닥 위에 있다 — Heisenberg 불확정성 원리는 정지한 입자를 허용하지 않는다
ZPE 공식
- $\text{ZPE} = \sum \tfrac{1}{2}h\nu_i$, 모든 실수 진동 모드에 대해 합산
- N–H, O–H (3000 cm⁻¹ 이상): 0.2–0.5 eV 기여
- 저주파수 제한된 모드 (200 cm⁻¹ 미만): 무시 가능
- 상태 간 ZPE 변화만 중요 (ΔZPE)
정량적 주의사항
- NH3 합성: ZPE 없이 0.83 eV 과도하게 발열 (Norskov 표 2.1)
- H 이동 반응: 항상 ZPE를 포함할 것
- 무시해도 되는 경우: H 이동이 없는 무거운 흡착종 (ΔZPE 0.05 eV 미만)
진동 엔트로피와 저주파수 보정
엔트로피: 다섯 가지 실용적 접근법
$\Delta S_{\text{ads}} = 0$으로 설정
엔트로피 차이가 0.05 eV 미만인 표면-표면 단계에서 정당화됨. 대규모 스크리닝에 빠르고 합리적. (Norskov CHE 2004)
$S_{\text{ads}} = 0.70 \cdot S_{\text{gas}}$
Campbell and Sellers, JACS 2012. 결합 강도에 따라 0.5–0.9 인자 적용. 이동성이 있는 물리흡착 또는 약하게 결합된 흡착종에 적합.
전체 조화 분배 함수 (ASE / VASPKIT)
T·S 오차는 일반적으로 표면 모드 기여의 30–50%. 화학흡착: T·S ~ 0.05–0.15 eV. 물리흡착: T·S ~ 0.3–0.5 eV로 오차가 훨씬 큼.
Ab initio MD (AIMD)
Born-Oppenheimer 또는 Car-Parrinello MD를 통해 유한 $T$에서 전체 퍼텐셜 에너지 표면을 샘플링. 비조화성과 확산을 자연스럽게 포착. 비용: 정적 DFT의 ~100–1000배; ps 시간 척도와 작은 셀로 제한됨.
MLIP 기반 MD
DFT 데이터로 훈련된 기계 학습 원자간 퍼텐셜 (MACE, NequIP, CHGNet 등). 고전 MD 비용으로 DFT에 근접한 정확도 — 열역학적 적분 또는 메타다이나믹스를 통한 수렴된 자유 에너지 샘플링을 위해 ns 시간 척도와 큰 슈퍼셀이 가능.
흡착종의 배치 엔트로피
$N$개의 흡착종이 $N_0$개의 표면 사이트를 점유하면 ($\theta = N/N_0$) 피복률에 의존하는 배치 엔트로피가 발생한다. *는 빈 사이트를 나타낸다.
중요한 경우
- $\theta$를 자기 일관적으로 풀는 미시 동역학 모델 (예: CatMAP)
- 다른 피복률의 표면을 비교하는 상 다이어그램
- $\theta = 0.5$일 때: $T \cdot s_{\text{config}} \sim 0.018$ eV (300 K), 0.059 eV (1000 K)
무시해도 되는 경우
- 같은 피복률에서 상태를 비교할 때 — $S_{\text{config}}$가 상쇄됨
- 희석 극한 ($\theta \to 0$) 또는 포화 ($\theta \to 1$)
- 대부분의 CHE 자유 에너지 다이어그램에서 의도적으로 생략됨
기상 열역학 예시
엔트로피와 엔탈피가 경쟁하는 곳
CO2 환원: 생성물 선택이 모든 것을 바꾸는 이유
298 K, pH 0에서의 평형 전위 vs. SHE
CO2 → CO (2e⁻)
TΔS ≈ 0 — 양쪽의 기체 몰수가 동일; 엔트로피가 도움을 주지 않음
CO2 → CH4 (8e⁻)
큰 유리한 ΔH가 엔트로피 벌칙을 압도; 전자당 열역학적으로 가장 용이
기상 기준 상태와 μ(T, P)
T 의존 항을 구하는 두 가지 경로
- ASE IdealGasThermo — DFT 진동 주파수를 사용
- NIST-JANAF 표 — 실험에서 직접 얻은 $[H(T) - H(298)]$과 $S(T)$를 표로 제공; DFT 주파수 불필요. 대부분의 일반적인 기체 분자를 포함 (H2, O2, H2O, CO2, NH3, CH4 등)
H2O 계산 예시
298.15 K, 1 bar에서
압력 항: $k_BT\ln(1/1) = 0$ eV
$\mu = E_{\text{DFT}} + \text{ZPE} + H_{\text{thermal}}(298) - 298 \cdot S(298)$
500 K, 0.01 bar에서
압력 보정: $0.04313\ln(0.01) = -0.20$ eV
$\mu$가 1 bar 대비 $-0.20$ eV 이동
상 다이어그램
반응 조건에서 어떤 상태가 가장 낮은 G를 갖는가?
제일원리로부터의 상 다이어그램
상 다이어그램은 T, P, pH, 또는 U의 함수로서 어떤 상태가 가장 낮은 G를 갖는지를 나타낸다. 안정성 경계: $\Delta G_{AB} = 0$
구성 방법
- 각 경쟁 상에 대해 $G(\text{variable})$를 작성
- 각 조건에서 가장 낮은 $G$ → 안정한 상
- 교차점이 안정성 경계를 정의
- 변수: $T, P(\text{O}_2)$; $U, \text{pH}$; $\mu_C, \mu_N$
예시: PdOx/CeO2 CH4 산화
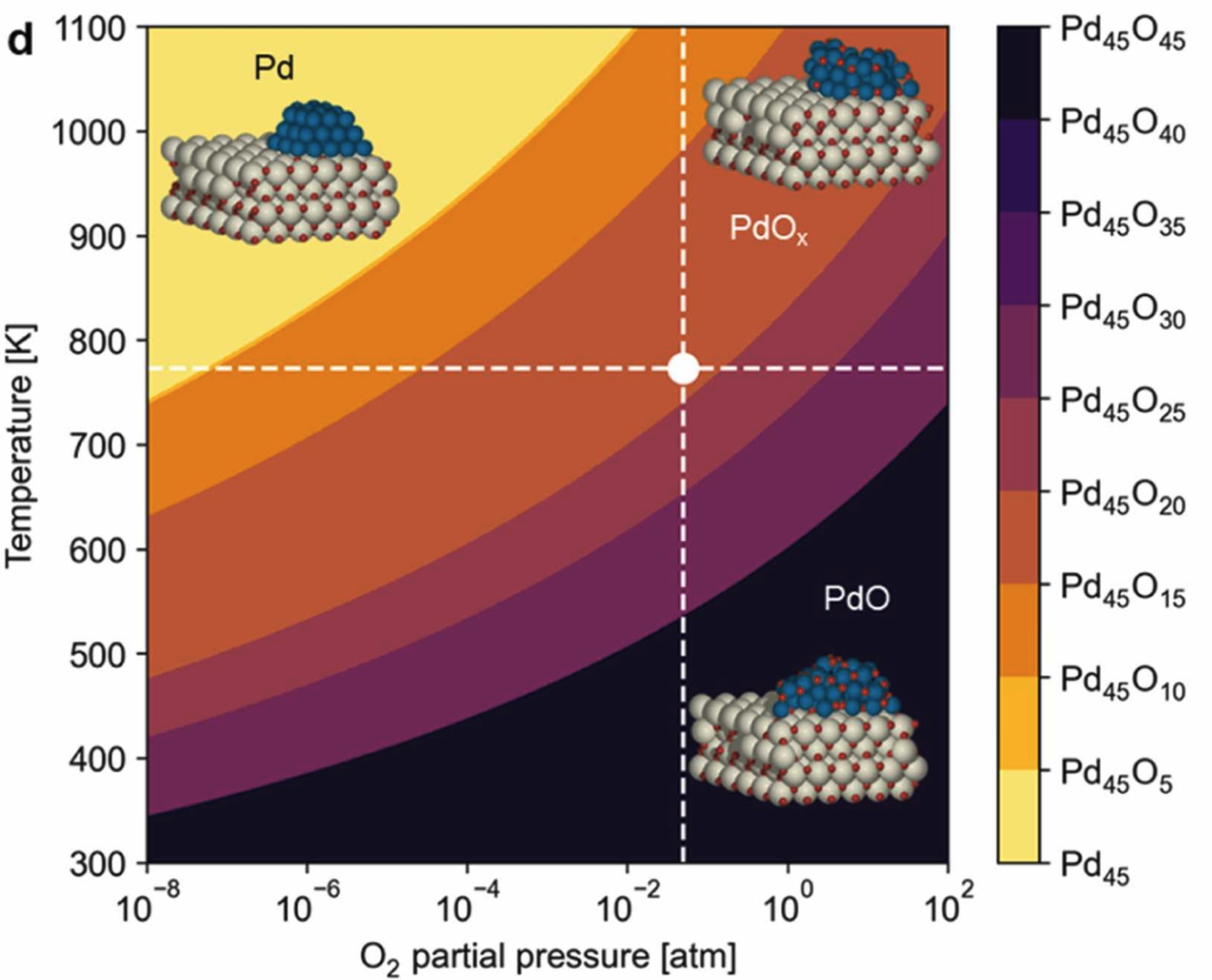
Ryu, Choung et al. Appl. Catal. B 379 (2025) 125672
$\Delta G_{\text{ox}}(T, P_{\text{O}_2}) = \Delta G_f^{\circ}(\text{PdO}) + \tfrac{1}{2}RT\ln(P_{\text{O}_2}/P_{\text{ref}})$
- 결함이 풍부한 CeO2는 Ce3+ 전자 공여를 통해 부분 환원된 PdOx를 안정화 — 경계를 더 높은 T로 이동
- 상 경계에서 활성 상태; 동적 산화환원 펄스가 일시적으로 이를 가로지름
표면 Pourbaix 다이어그램
구성 방법
- 각 표면 상태에 대해 $G(U, \text{pH})$를 작성. 기울기는 $n$ (이동된 전자 수)에 의해 결정.
- 각 $U$에서 가장 낮은 선이 안정함. 교차점 → 상 경계.
- 2D 맵을 위해 pH 0–14를 스윕. pH는 298 K에서 0.0592 V/pH만큼 이동.
예시: Fe(OH)x/Pt ORR
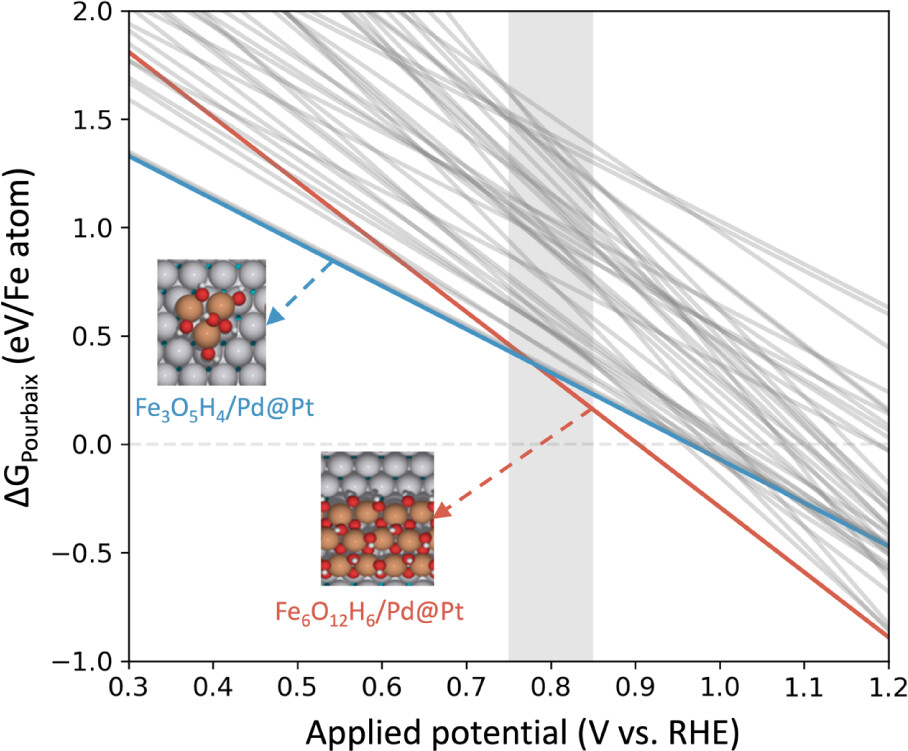
Maiti, Choung et al. ACS Appl. Mater. Interfaces 17 (2025) 40517
- ORR 조건 (0.7–0.9 V vs. RHE)에서: Fe3+(OH)3 또는 FeOOH가 안정 — 금속 Fe가 아님
- Pt 기판이 전하 이동을 통해 벌크 Fe Pourbaix 대비 경계를 이동시킴
- 작동 전위에서 Fe3+ 산화 상태를 고정하도록 계면을 설계
예시 3: Fe-Ce 산화물 위 Rh SAC 안정성
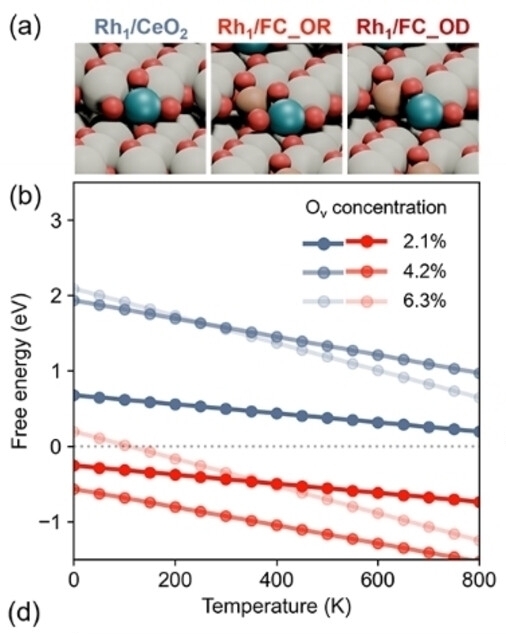
Kim, Choung et al. Angew. Chem. Int. Ed. 64 (2025) e202421218
Rh+ SAC가 반응 조건에서 Rh⁰로의 소결 대비 안정하게 유지되는가?
경쟁 상태: Rh+/결함, Rh3+/화학량론적, Rh⁰ 클러스터, 용해된 Rhn+
- Ce3+ 결함은 Rh+를 화학량론적 사이트보다 ~0.5–1.0 eV 더 강하게 결합
- 결함이 풍부한 Fe-Ce 산화물은 높은 T에서 더 낮은 P(O2)까지 Rh+ SAC 안정성 영역을 확장
- 상 다이어그램이 소결 저항성을 직접 예측 — 내구성 실험으로 확인됨
- 결함이 풍부한 지지체에서만 작동점이 SAC 안정 영역 내에 있음
전기화학과 CHE
계산적 수소 전극
전기화학에서의 자유 에너지: CHE 모델
Norskov et al. (2004): U = 0 V vs. RHE에서, G(H⁺ + e⁻) = ½G(H2). U를 −eU만큼 이동하면 모든 전자 이동 단계가 이동한다.
ORR 계산 예시: 단계별 자유 에너지 다이어그램
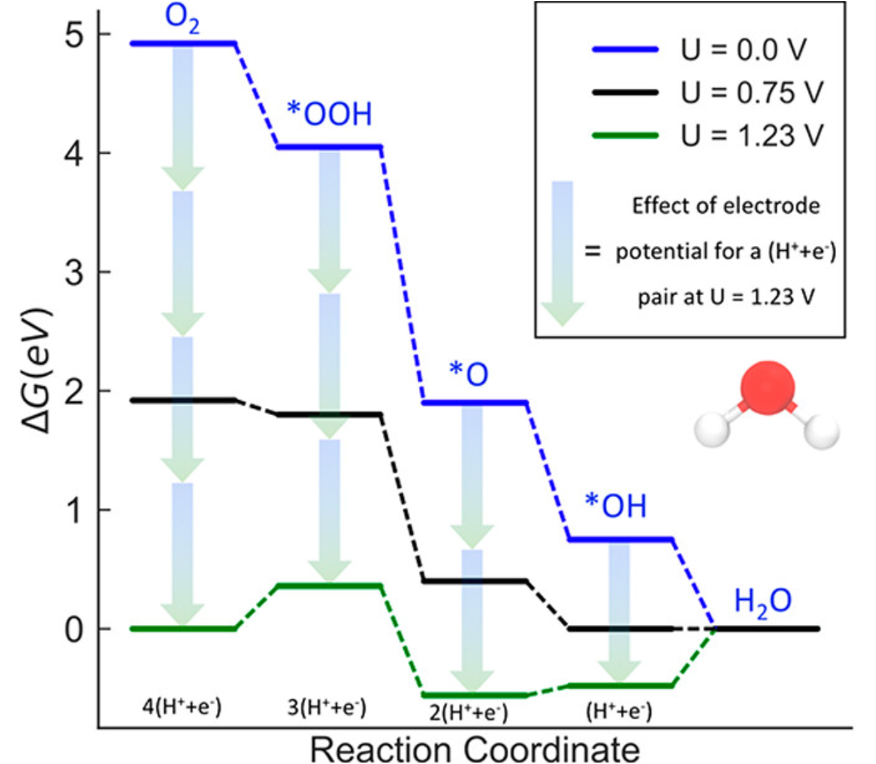
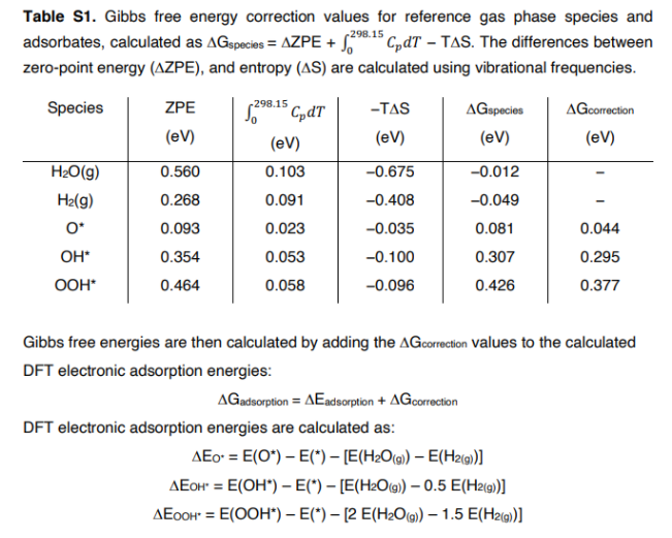
O2 + 4(H⁺ + e⁻) → 2H2O | Pt(111)에서의 4단계 결합 메커니즘
자유 에너지 계산이 얼마나 틀릴 수 있는가?
오차 단계: 범함수, 모델, 열적, 사이트 선택
오차 단계 1: DFT 범함수
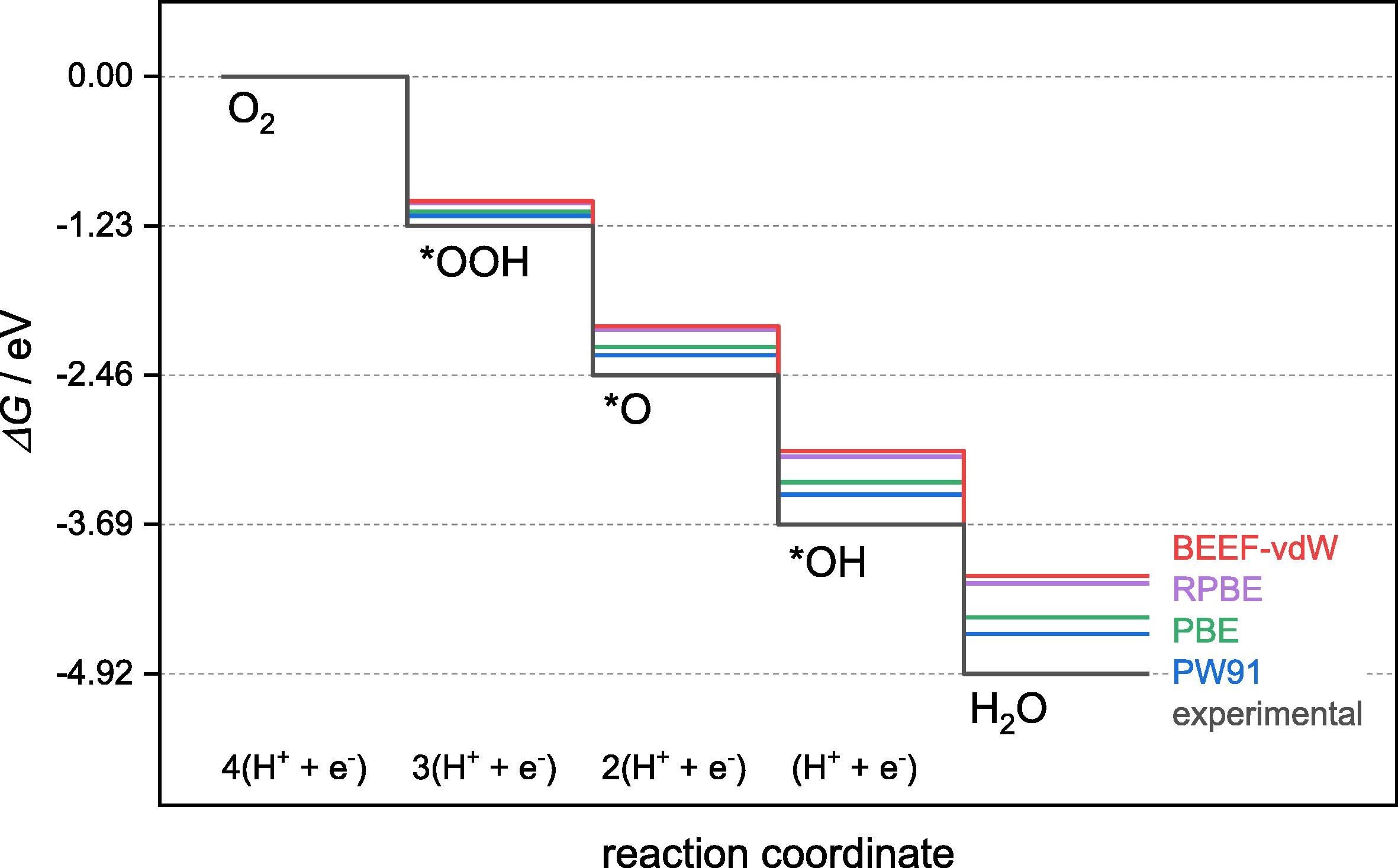
Sargeant, Illas, Rodríguez & Calle-Vallejo, J. Electroanal. Chem. 896 (2021) 115178
GGA-PBE는 O 함유 흡착종을 과결합함
금속 위 O*, OH*, OOH*에 대한 체계적 오차 0.2-0.4 eV. 무작위가 아님 — 유사한 흡착종 간에 상관되어 있어 화산 플롯은 여전히 촉매를 올바르게 순위 매김. 절대 과전위는 0.2-0.4 V 오차가 있을 수 있음.
주의할 때
- 실험 대비 절대 흡착 에너지
- 서로 다른 작용기 비교 (O vs. N 흡착종)
- 산화물 — GGA+U 또는 HSE06 필요
오차가 상쇄될 때
- 같은 흡착종 계열 내의 상대 에너지
- 화산 플롯 순위 (오차가 상관됨)
- 스케일링 관계 기울기 (범함수에 거의 무관)
오차 단계 2: 모델과 설정
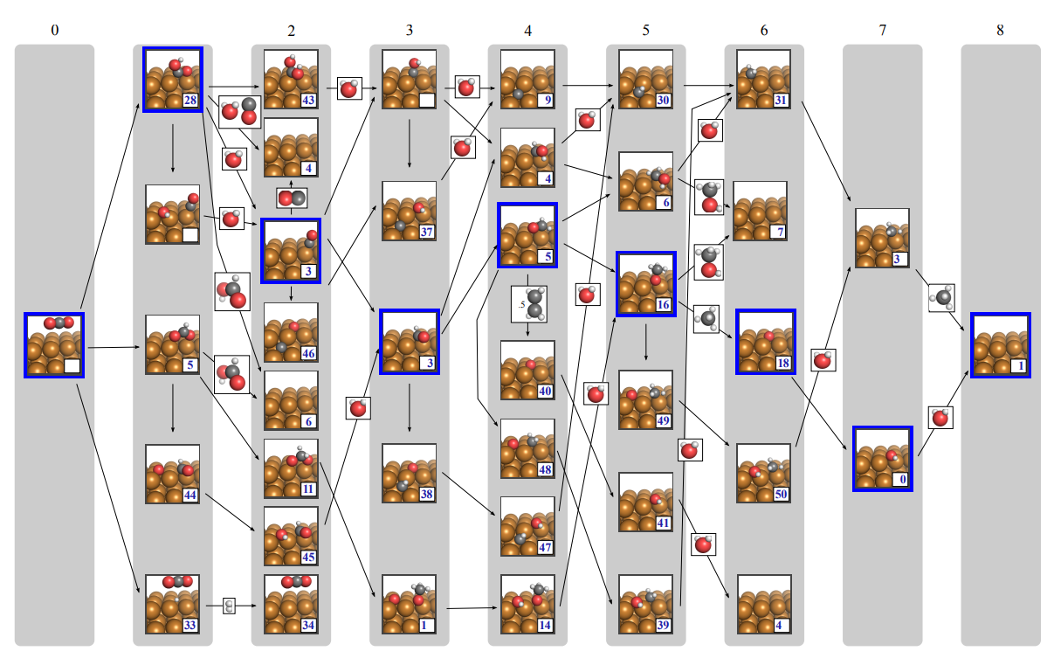
오차 단계 3: 어떤 사이트를 모델링했는가?

Govindarajan, Kastlunger, Heenen & Chan, Chem. Sci. 2022, 13, 14–26
- DFT 스크리닝은 일반적으로 하나의 결합 사이트를 선택한다. 선택한 사이트가 동역학적으로 지배적인 사이트가 아니면, 수치적 정확도와 무관하게 예측이 실패한다.
- Au(111) Pb-UPD 등고선 분석 (Nitopi et al., Chem. Sci. 2022): 테라스와 저배위 사이트 간 80-120 meV 장벽 차이가 Arrhenius를 통해 저배위 사이트에서 20-100배 높은 TOF로 변환됨.
- Co 산화물 OER: 소수 결함 사이트가 평균 Co 표면 사이트보다 100배 높은 TOF를 보임 (Frei 시간 분해 FTIR; Plaisance 미시 동역학 모델링). 지배적인 활성 사이트는 인가 전위에 따라 변화함.
- 0.10 eV 장벽 차이는 일반적인 DFT 오차 범위보다 작지만, 속도를 제어하는 사이트를 1-2 자릿수 변화시킨다. 사이트 정량 (Pb-UPD, 산화환원 피크 적분, CO/CN 프로브)이 필수적이다.
- 완벽한 DFT 동역학조차 실험에서 물질 전달 제한(H2, O2, CO2의 낮은 용해도)에 의해 가려질 수 있다.
자주 묻는 질문
자유 에너지 계산에 대한 흔한 질문들
언제 ZPE와 엔트로피를 안전하게 무시할 수 있는가?
- H 이동이 없고 반응물/생성물 질량이 유사한 표면-표면 단계 — ΔG ~ ΔE, ~0.05 eV 이내
- 절대값보다 경향이 더 중요한 대규모 촉매 라이브러리 스크리닝 (수백 개의 재료)
- 유사한 금속 위 같은 흡착종 계열 내 비교 — 차이에서 오차가 상쇄됨
- 400 K 이상의 기상 반응: 엔트로피는 절대 무시할 수 없음 — NIST 열화학 표를 사용
- 전기화학의 경우: CHE는 H2 기준을 통해 기상 T·S를 처리하지만, 표면 T·S는 속도 결정 단계에서 여전히 중요
어떤 엔트로피 접근법을 사용해야 하는가?
표면-표면 단계; 빠른 스크리닝
반응물과 생성물 모두 화학흡착일 때 ΔS ~ 0. T*ΔS 0.05 eV 미만. 대규모 DFT + CHE 스크리닝의 기본값.
물리흡착 또는 약하게 결합된 중간체
이동성 있는 흡착종 (표면 위 큰 분자, 물리흡착). 결합 에너지에 따라 Campbell 인자 0.5-0.9. 빠른 추정.
속도 결정 단계, 검증, 논문 발표
ASE HarmonicThermo 또는 VASPKIT 501을 사용. 100 cm⁻¹ 미만 모드에 대한 quasi-RRHO 보정을 보고할 것. 정량적 과전위 주장에 필수적.
CHE 모델의 한계는 무엇인가?
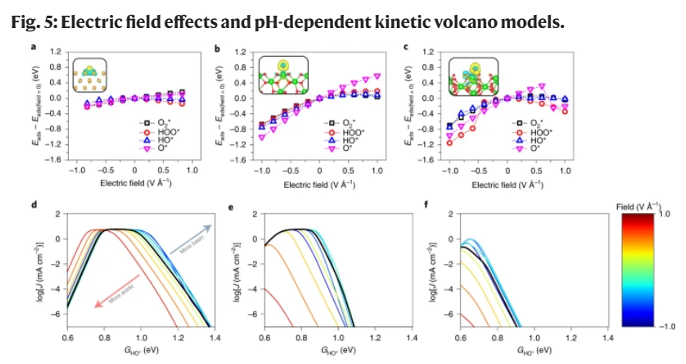
- 동역학적 장벽 없음 — CHE는 순수 열역학적; 실제 장벽은 0.3-0.8 eV 다를 수 있음
- 명시적 용매 없음 — 묵시적 용매화는 극성 중간체에 대해 ΔG를 0.1-0.3 eV 이동시킬 수 있음
- 피복률 의존성 없음 — 측면 상호작용이 개시 전위를 0.1-0.2 V 이동시킴
- Frumkin 보정 없음 — 이상적인 이중층을 가정; 높은 과전위에서 실패
- Grotthuss 호핑을 포함하는 양성자 이동 단계에 부적합 — 명시적 물 분자 필요
올바른 기준 상태를 어떻게 설정하는가?
- 모든 에너지를 같은 화학 퍼텐셜로 기준화할 것: H → ½G(H2), O → G(H2O) − G(H2), C → G(CO2) − G(O2)
- 같은 경로에서 DFT로 계산한 기상 G와 실험적 엔탈피를 혼합하지 말 것
- 슈퍼셀 크기는 절대 표면 에너지에 영향을 주지만, 슬랩이 수렴되면 화학흡착의 ΔG에는 영향을 주지 않음
- 상 다이어그램의 경우: μO(T, P) = ½G(O2) + ΔμO(T, P)를 NIST-JANAF 또는 포논 계산에서 설정
자유 에너지 불확도를 어떻게 추정하고 보고해야 하는가?
- DFT 범함수: 금속 위 O* 계열에 대해 +/- 0.2-0.4 eV (PBE); 해당 시스템에 대한 체계적 벤치마크를 인용할 것
- 열적 보정: 300 K에서 화학흡착에 대해 +/- 0.05 eV; 물리흡착 또는 T 700 K 이상에서 +/- 0.15 eV
- 모델 설정: 슬랩 두께, k-메쉬, ENCUT를 체계적으로 수렴시키고 수렴 기준을 명시적으로 보고
- 오차 전파: 다단계 경로에 대해 선형 오차 전파를 사용; $\sigma_{\text{total}} = \sqrt{\sum \sigma_i^2}$
EDFT는 사진이다. G(T,P)는 영화이다.
자유 에너지는 실제로 일어나는 일의 전체 이야기를 담고 있다
모든 보정이 중요하다
무엇을 무시하는지, 왜 무시하는지 알아야 한다
상 다이어그램은 거짓말하지 않는다
과감하게 계산하고, 신중하게 보정하고, 정직하게 해석하라.